مقدمه
سرطان یکی از مهمترین چالشهای سلامت عمومی در قرن حاضر به شمار میرود و سالانه میلیونها نفر را در سراسر جهان درگیر میسازد. این بیماری نه تنها تهدیدی جدی برای بقای فردی است، بلکه اثرات اجتماعی و اقتصادی گستردهای نیز به همراه دارد. برای درک دقیق ماهیت سرطان، شناخت سازوکارهای زیستی حاکم بر چرخه سلولی و تغییرات ژنتیکی ضروری است. چرخه سلولی به عنوان یک برنامه تنظیمشده، تقسیم سلول را تحت کنترل دقیق نقاط نظارتی قرار میدهد. هرگونه اختلال در این نقاط یا تغییر در ژنهای تنظیمکننده، میتواند منجر به رشد بیرویه سلول و در نهایت شکلگیری تومور گردد.
طی دهههای اخیر، پژوهشگران موفق شدهاند ویژگیهای اصلی سلولهای سرطانی را شناسایی کنند؛ از جمله توانایی رشد مستقل از سیگنالهای بیرونی، بیتوجهی به سیگنالهای بازدارنده، فرار از آپوپتوز، تقسیم نامحدود، القای آنژیوژنز و قابلیت متاستاز. شناخت این ویژگیها، راه را برای ابداع روشهای نوین تشخیص و درمان هموار ساخته و امید به کنترل این بیماری پیچیده را افزایش داده است.
چرخه طبیعی سلول و اهمیت کنترل آن
چرخه سلولی فرآنندی تکراری است که در آن سلول ابتدا رشد میکند، DNA خود را همانندسازی مینماید و سپس تقسیم میشود. این چرخه شامل چهار مرحله اصلی است:
- مرحله G1 : سلول رشد میکند، پروتئینهای لازم را میسازد و شرایط محیطی و داخلی را برای تکثیر بررسی میکند.
- مرحله S: در این مرحله از DNA همانندسازی میشود. این مرحله بسیار حساس است زیرا کوچکترین خطا در کپیبرداری DNA میتواند منجر به جهش شود.
- مرحله G2 : سلول بررسی میکند که DNA بدون خطا تکثیر شده و آماده ورود به تقسیم نهایی باشد.
- مرحله M : تقسیم هسته و سپس کل سلول اتفاق میافتد و دو سلول دختر حاصل میشود.
علاوهبراین مراحل، سلولها ممکن است وارد وضعیت G0 شوند. در این حالت سلول در چرخه تقسیم فعال نیست و در حالت استراحت قرار دارد. بسیاری از سلولهای بدن مانند سلولهای عصبی و ماهیچهای در این وضعیت باقی میمانند.
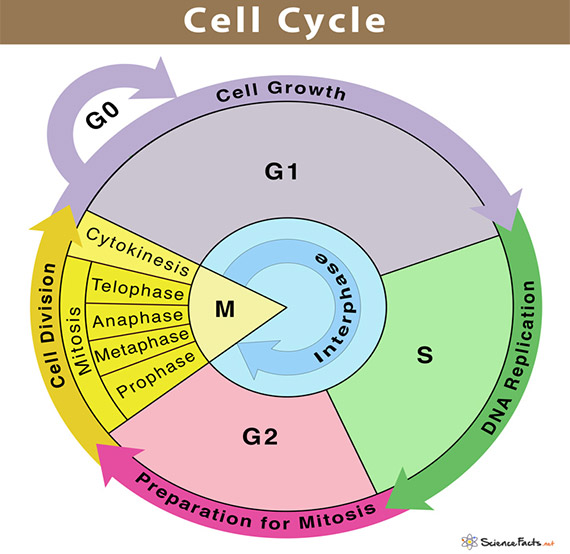
مرحله G0 نیز حالتی غیرتقسیمی است که سلول وارد استراحت یا فعالیت تخصصی میشود.
نقاط بازرسی و پروتئینهای کلیدی
چرخه سلولی توسط نقاط کنترلی (Checkpoints) تنظیم میشود. این نقاط مانند ایستگاههای بازرسی عمل میکنند و مانع ورود سلول به مرحله بعدی در صورت وجود خطا میشوند. مهمترین نقاط کنترلی عبارتاند از:
- نقطه کنترل G1/S : بررسی وجود مواد مغذی، سیگنالهای رشد و سلامت DNA
- نقطه کنترل G2/M : اطمینان از تکثیر صحیح DNA
- نقطه کنترل دوکها (Spindle checkpoint ): بررسی اتصال صحیح کروموزومها به میکروتوبولهای دوک تقسیم
این کنترلها تحت نظارت پروتئینهای ویژهای مانند سیکلینها (Cyclins) و کینازهای وابسته به سیکلین (CDKs) هستند. سیکلینها با تغییر غلظت خود در طول چرخه سلولی، فعالیت CDKها را تنظیم میکنند. CDKها نیز با فسفریلاسیون پروتئینهای هدف، مسیر ورود سلول به مراحل بعدی را فعال یا مهار میکنند.
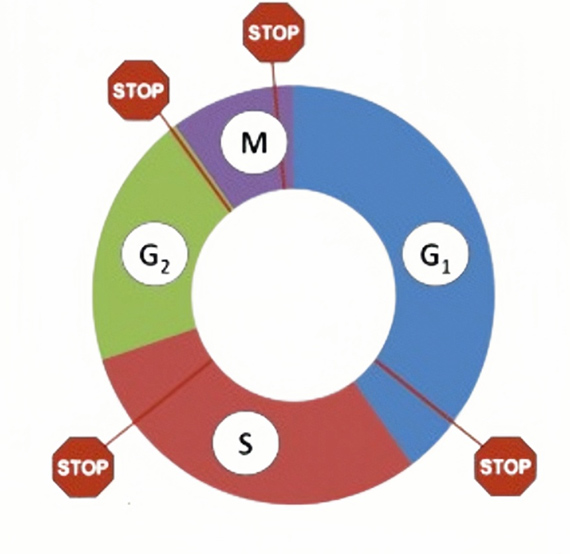
نقاط کنترل در مراحل G1، S، G2 و M قرار دارند و از ورود سلولهای دارای خطا به مرحله بعدی جلوگیری میکنند تا تقسیم سلولی سالم انجام شود.
تغییرات ژنتیکی در سرطان
سرطان نتیجه انباشت تدریجی جهشهای ژنتیکی است. این جهشها میتوانند ناشی از عوامل محیطی مانند اشعهها و مواد شیمیایی سرطانزا باشند یا در اثر خطاهای داخلی طی همانندسازی DNA ایجاد شوند.
ژنهای سرکوبگر تومور
این ژنها همانند ترمز خودرو عمل میکنند و تقسیم سلول را محدود میسازند. اگر این ژنها غیرفعال شوند، کنترل رشد از دست میرود. از مهمترین ژنهای سرکوبگر تومور میتوان به موارد زیر اشاره کرد:
- P53 : معروف به “نگهبان ژنوم” که وظیفه توقف چرخه سلولی در صورت آسیب DNA یا القای آپوپتوز را دارد. بیش از نیمی از سرطانها با جهش در این ژن مرتبط اند.
- Rb(Retinoblastoma protein ) : تنظیمکننده ورود سلول از مرحله G1 به S است. غیرفعال شدن Rb باعث تکثیر کنترلنشده میشود.
پروتوانکوژنها و انکوژنها
پروتوانکوژنها ژنهایی طبیعی هستند که در شرایط عادی رشد سلولی را تحریک میکنند. اما وقتی دچار جهش میشوند یا بیشازحد فعال میشوند، به انکوژن تبدیل میشوند. نمونههایی از انکوژنها عبارتانداز:
- RAS: پروتئینی در مسیر پیامرسانی که در صورت جهش، رشد سلولی دائماً فعال باقی میماند.
- MYC: فاکتور رونویسی که بیان ژنها مرتبط با رشد را افزایش میدهد.
فرار از مرگ برنامهریزیشده (آپوپتوز)
یکی از ویژگیهای سلولهای طبیعی توانایی نابودی خود در صورت آسیب جدی است. این فرآیند آپوپتوز نام دارد و توسط پروتئینهای خانواده BCL-2 و کاسپازها کنترل میشود. سلولهای سرطانی با افزایش بیان پروتئینهای ضدآپوپتوز( مانند BCL-2 ) یا کاهش پروتئینهای پروآپوپتوتیک، از مرگ میگریزند و به بقا ادامه میدهند.

این مکانیسم نقش مهمی در رشد، تکامل و پیشگیری از بروز بیماریهایی مانند سرطان دارد.
تقسیم بینهایت و تلومراز
سلول های طبیعی محدودیت تقسیم دارند که به آن حد هایفلیک گفته می شود. علت این کوتاه شدن تدریجی تلومرها است. سلولهای سرطانی با فعال سازی آنزیم تلومراز، تلومرها را بازسازی کرده و توانایی تقسیم نامحدود پیدا میکنند.
آنژیوژنز و متاستاز
تومورها برای رشد بیش از چند میلیمتر به اکسیژن و مواد غذایی بیشتری نیاز دارند. برای این منظور با ترشح فاکتورهایی مانند VEGF ( Vascular Endothelial Growth Factor ) رگهای خونی تازه ایجاد میکنند. این فرایند آنژیوژنز نام دارد.
همچنین سلولهای سرطانی میتوانند به بافتهای اطراف نفوذ کنند، وارد جریان خون یا لنف شوند و به نقاط دوردست بدن برسند. این فرآیند متاستاز نام دارد که مسئول بیشتر مرگومیر ناشی از سرطان است. متاستاز نیازمند تغییراتی در چسبندگی سلولی، توانایی حرکت و مقاومت در برابر شرایط جدید است.
ویژگیهای بنیادی سلولهای سرطانی
پژوهشها نشان دادهاند که سلولهای سرطانی برای بقا و پیشرفت خود مجموعهای از ویژگیهای اساسی را کسب میکنند که به آنها «نشانههای اصلی سرطان» گفته میشود. این تواناییها شامل موارد زیر است:
- ایجاد و حفظ سیگنالهای رشد بدون نیاز به محرکهای بیرونی
- نادیده گرفتن پیامهای مهارکننده رشد
- گریز از فرایند مرگ برنامهریزیشده سلولی (آپوپتوز)
- توانایی تقسیم و تکثیر بیپایان
- تحریک رگزایی (آنژیوژنز) برای تأمین خون و مواد غذایی
- قابلیت نفوذ به بافتهای اطراف و گسترش به نقاط دورتر بدن (متاستاز)
با گذشت زمان و پیشرفت دانش زیستپزشکی، ویژگیهای دیگری نیز به این فهرست افزوده شده است؛ از جمله توانایی فرار از شناسایی و تخریب توسط سیستم ایمنی و تغییر در متابولیسم سلولی برای سازگاری با شرایط جدید میتوان نام برد.
عوامل خطر و زمینههای بروز سرطان
علتهای پیدایش سرطان را میتوان در دو گروه اصلی جای داد:
- عوامل محیطی یا بیرونی: موادی و شرایطی که از خارج بر بدن اثر میگذارند،از جمله مصرف دخانیات و الکل، قرار گرفتن در معرض پرتوهای فرابنفش، آلودگیهای شیمیایی و صنعتی، و همچنین برخی عفونتهای ویروسی نظیر ویروس پاپیلومای انسانی (HPV) و ویروس هپاتیت B اشاره کرد.
- عوامل درونی یا ژنتیکی : عواملی که ریشه در ساختار و عملکرد داخلی بدن دارند، از جمله میتوان به جهشهای ارثی، تغییرات هورمونی، ضعف یا اختلال در دستگاه ایمنی و خطاهای ایجادشده هنگام همانندسازی DNA اشاره کرد.
در بیشتر موارد، سرطان نتیجه تأثیر همزمان و تدریجی این دو گروه عامل است که با انباشت جهشها و تغییرات ژنتیکی، زمینه تشکیل و رشد تومور را فراهم میسازد.
تشخیص و درمان سرطان
شناخت بهموقع سرطان نقش تعیینکنندهای در موفقیت درمان دارد. برای شناسایی زودهنگام، از روشهای مختلفی استفاده میشود؛ از جمله آزمایشهای خونی برای کشف تغییرات غیرطبیعی، روشهای تصویربرداری مانند سیتیاسکن (CT) و امآرآی (MRI) برای بررسی دقیق بافتها، و در نهایت نمونهبرداری یا بیوپسی که معتبرترین راه برای تشخیص نوع و ماهیت تومور است.
پس از تشخیص، انتخاب شیوه درمان وابسته به نوع سرطان، محل آن و میزان پیشرفت بیماری است. مهمترین روشهای درمانی عبارتاند از:
- جراحی: حذف توده سرطانی از بدن.
- شیمی درمانی: بهکارگیری داروهایی که سلولهای در حال تقسیم را تخریب یا مهار میکنند.
- پرتودرمانی: استفاده از اشعه برای آسیبزدن به DNA سلولهای سرطانی و متوقف ساختن رشد آنها.
- ایمونوتراپی: تحریک و تقویت سیستم ایمنی بدن تا بتواند سلولهای بدخیم را بهتر شناسایی و نابود کند.
- درمانهای هدفمند: داروهایی نوین که به طور اختصاصی روی پروتئینها یا مسیرهای مولکولی معیوب در سلولهای سرطانی اثر میگذارند.
این مجموعه روشها اغلب به صورت ترکیبی مورد استفاده قرار میگیرند تا اثربخشی درمان افزایش بابد و احتمال بازگشت بیماری کاهش پیدا کند.
پیشگیری و سبک زندگی سالم
هرچند درمان سرطان پیچیده است، اما پیشگیری میتواند نقش بزرگی در کاهش بروز آن داشته باشد. ترک سیگار، تغذیه سالم با مصرف میوهها و سبزیجات تازه، فعالیت بدنی منظم، پرهیز از مواجهه طولانی با نور خورشید، واکسیناسیون علیه ویروسهای سرطانزا و غربالگریهای دورهای از جمله اقدامات مؤثر در پیشگیری هستند.

نتیجهگیری
سرطان حاصل تجمع تغییرات ژنتیکی و برهم خوردن نظم چرخه طبیعی سلول است. سلولهای سرطانی با رهایی از کنترل رشد، گریز از مرگ برنامهریزیشده، فعالسازی آنزیم تلومراز، توانایی ایجاد رگهای خونی تازه و قابلیت گسترش به بافتهای دوردست، ماهیتی متفاوت و تهدیدکننده پیدا میکنند. درک عمیق این فرایندها نه تنها برای شناخت ذات سرطان اهمیت دارد، بلکه زیربنای توسعه راهکارهای نوین در پیشگیری، تشخیص زودهنگام و درمان مؤثر آن به شمار میآید. دستاوردهای علمی نوید میدهند که در آینده بتوان این بیماری پیچیده را نه به عنوان تهدیدی مرگبار، بلکه بهعنوان اختلالی قابل مهار و حتی درمانپذیر مدیریت کرد.
منابع
نویسنده: نسترن قادرپوریان